ПРОБЛЕМНІ СТАТТІ
УДК 613.6/612.017:616.15:615:001.5
И.М. Трахтенберг, академик АМНУ, О.В. Ермакова, И.П. Лубянова, к.м.н.
СОВРЕМЕННЫЕ АСПЕКТЫ ПРИМЕНЕНИЯ a-ЛИПОЕВОЙ КИСЛОТЫ ПРИ ЭКЗОГЕННЫХ ТОКСИЧЕСКИХ ВОЗДЕЙСТВИЯХ
(Обзор литературы)
Институт медицины труда, г. Киев
Первые сообщения о терапевтическом применении липоевой кислоты сделал Coralusso u Rauch на Международном симпозиуме по тиоктовой кислоте в Токио в 1955 году [18].
Были отмечены хорошие результаты применения препарата при лечении болезней печени (включая печеночную кому), сахарного диабета, атеросклероза и ряда интоксикаций (прежде всего гепатотоксическими ядами) [17]. Благодаря свойствам липоевой кислоты восстанавливать запасы глутатитона, предотвращать повреждение митохондрий, высвобождение и гибель клеток, обусловленную воздействием фактора некроза опухоли (TNF-g), a-липоевая кислота нашла широкое применение в гастроэнтерологии, эндокринологии, кардиологии.
Кислота липоевая (Acidum lipoicum) — 6,8-дитиооктановая кислота. Синонимы: Acidum thiocticum, Biletan, Heparlipon, Protogen, Thioctacid, Thioctan, Tioctacid, Tioctan, липоновая кислота, тиокаприловая кислота и др. Кристаллический порошок светло-желтого цвета, горьковатого вкуса, со специфическим запахом. Практически нерастворим в воде, легко растворим в спирте. Натриевая соль липоевой кислоты хорошо растворяется в воде. Липоевая кислота является коферментом, участвующим в окислительном декарбоксилировании пировиноградной кислоты и a-кетокислот, и играет существенную роль в процессе образования энергии в организме. По характеру биохимического действия липоевая кислота приближается к витаминам группы В. Альфа-липоевая кислота (a-липоевая кислота) была открыта в 1948 году О'Кейном и Гунсалусом. Впервые a-липоевая кислота была выделена в кристаллическом виде из экстракта говяжьей печени в 1951 году группой ученых во главе с американским биохимиком Л. Ридом. В 1952 году была расшифрована структура a-липоевой кислоты, которая представляет собой 1,2-дитиолан-3-валериановую кислоту.
Молекула a-липоевой кислоты состоит из 8-атомной углеродной цепи с двумя атомами серы. В молекуле этой кислоты был обнаружен один хиральный атом углерода, и поэтому существует две энантиомерные формы. В лечебных целях используют рацемат M- и S-формы.
Структурная формула a-липоевой кислоты (a) представлена пятичленным гетероциклическим кольцом. При разрушении дисульфидного мостика внутри кольца образуется дигидролипоевая кислота (b). При растворении это соединение под действием света и кислорода легко полимеризуется.
Деформация в пятичленном дисульфидном кольце обуслoвливает тесную корреляцию между химическим строением a-липоевой кислоты и ее биологической активностью.
Структурные формулы:
а) альфа-липоевая кислота
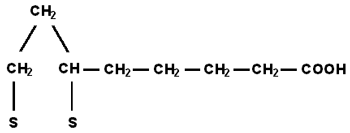
b) дигидролипоевая кислота
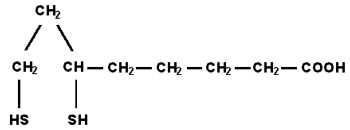
Эмпирическая формула: С8H14O2S2.
Молекулярная масса: 206,32.
Внешний вид: желтый кристаллический порошок.
Точка плавления: 60—61°C.
Растворимость: слабо растворим в воде, D-, L-форма легко растворима в липофильных растворителях с образованием соли натрия, легко растворимой в воде.
В соответствии с современными представлениям, a-липоевую кислоту классифицируют как витаминоид. Ее биосинтез может осуществляться не только в бактериях и растениях, но и в высших организмах. В настоящее время вопрос, является ли a-липоевая кислота незаменимой для человека, остается открытым [19].
Липоевая кислота участвует в аэробном окислении углеводов, играя роль своего рода переносчика водорода в процессе попеременного превращения в дисульфидную и в сульфгидрильную форму.
Альфа-липоевая кислота играет достаточно важную роль в утилизации сахаров и осуществлении нормального энергетического обмена. Через e-аминогруппу лизинового остатка она связывается с центральным компонентом ацилтрансферазы и действует как кофермент в таких многоферментных комплексах митохондрий, как:
а) пируватдегидрогеназный комплекс (катализирует превращение пирувата в ацетил-КоА);
b) альфа-оксиглютаратдегидрогеназа (фермент в цикле лимонной кислоты);
c) дегидрогеназа аминокислот с разветвленной цепью.
Будучи активным метаболитом, a-липоевая кислота имеет широкий спектр биологического и фармакологического действия. Это обусловлено её участием в процессах окислительного декарбоксилирования пировиноградной и кетоглутаровой альфа-кислот, протекающих в матриксе митохондрий. Облегчая превращение молочной кислоты в пировиноградную с последующим декарбоксилированием последней, a-липоевая кислота способствует ликвидации метаболического ацидоза. Содействуя образованию коэнзима А (КоА), она облегчает перенос ацетата и жирных кислот из цитозоля в матрикс митохондрий для последующего окисления. Это сопровождается уменьшением выраженности жировой дистрофии гепатоцитов, активизацией метаболической функции печени и желчеотделения. Кроме того, a-липоевая кислота ускоряет окисление жирных кислот, оказывая гиполипидемическое действие [18].
Было доказано, что липоевая кислота, снижая содержание аммиака в крови, уменьшает проявления печеночной энцефалопатии у больных с гипераммониемией, обусловленной прямым портокавальным анастомозом. Положительный терапевтический эффект отмечен на
Берлитион обладает выраженным иммуномодулирующим свойством. При приёме a-липоевой кислоты активируется фагоцитоз нейтрофилов и повышается уровень комплемента. Радиопротекторный эффект берлитиона обусловлен его антирадикальными свойствами. Это даёт возможность широко и эффективно применять берлитион у пострадавших от ионизирующего облучения [3].
Таким образом, основными биологическими свойствами липоевой кислоты являются:
- улучшение трансмембранного транспорта глюкозы с активацией процессов окисления глюкозы;
- снижение интенсивности процессов гликолизирования белка;
- антиоксидантный эффект;
- снижение концентрации жирных кислот в плазме;
- подавление процессов липолиза;
- снижение содержания общего уровня холестерина и его эфиров в крови;
- увеличение уровня протеинов в сыворотке крови;
- радиопротекторное действие (за счёт антирадикальных свойств);
- предупреждение ингибирования активности NO;
- потенцирование противовоспалительного действия глюкокортикостероидов;
- желчегонный, детоксицирующий и спазмолитический эффекты;
- способность к обратимому связыванию молекул ДНК.
С развитием современных представлений об "окислительном стрессе" и перекисном окислении липидов (ПОЛ) как об универсальном механизме повреждения клеток и тканей связано формирование новых подходов в лечении заболеваний дисметаболической природы. Антиоксидантный эффект a-липоевой кислоты обусловлен наличием двух тиоловых групп в молекуле, а также способностью связывать молекулы радикалов и свободное тканевое железо (предотвращая его участие в ПОЛ). Получены доказательства о том, что a-липоевая кислота не только обладает самостоятельным антиоксидантным потенциалом, но и обеспечивает мощную поддержку работы других антиоксидантных звеньев в организме. В этом отношении её протективное действие тесно связано с гомеостазом в системе глутатиона и убихинона.
Предполагается, что процесс старения во многом обусловлен механизмами окислительного повреждения клеточных структур и активных центров ферментов, что сопровождается уменьшением их сродства к субстратам. Применение a-липоевой кислоты способствует восстановлению функции митохондрий и уменьшению накопления прооксидантов [18].
Окислительный стресс является центральным патогенетическим звеном в генезе диабетической невропатии. С одной стороны, в результате протекания реакций гликолиза и расстройства эндоневрального кровообращения усиливается перекисное окисление с образованием свободных радикалов, а с другой, — снижается эффективность работы системы антиоксидантной защиты.
Образование свободных радикалов происходит и при нормальных физиологических условиях, однако в этом случае они немедленно "нейтрализуются" системой антиоксидантной защиты. Эта система включает витамины Е, С, глютатион, НАДН/НАДФН, а также a-липоевую кислоту.
Увеличение количества свободных радикалов происходит также и вследствие гликолиза белков с образованием конечных продуктов гликолиза, которым отводится решающая роль в развитии и прогрессировании невропатии и других вторичных повреждений при диабете. Гликолиз матричных белков сосудистого эндотелия приводит к увеличению сопротивления потоку крови в мелких сосудах и, следовательно, вызывает изменение кровотока. Таким образом, возникает порочный круг: расстройство эндоневрального кровообращения приводит к образованию свободных радикалов, которые, в свою очередь, могут вызывать дальнейшее повреждение сосудистого эндотелия.
В организме a-липоевая кислота действует в качестве резервной системы для запуска важных антиоксидантов и, кроме того, сама по себе является эффективной "ловушкой" для радикалов. Альфа-липоевую кислоту и ее восстановленную форму называют "универсальным антиоксидантом", который функционирует как на мембране, так и в водных средах. Таким образом, антиоксидантный эффект a-липоевой кислоты можно объяснить тем, что она:
- предотвращает модификацию белков, вызванную действием глюкозы;
- увеличивает сниженный эндоневральный кровоток;
- при невропатии компенсирует недостаток глютатиона в нервных клетках;
- снижает концентрацию диеновых конъюгатов, образующихся вследствие перекисного окисления липидов;
- нормализует проводимость по нервным волокнам.
Антиоксидантные свойства a-липоевой кислоты объясняются её способностью переводить Fe2+ в Fe3– [20], а также хелатировать Fe2+, Cu2+ (дигидролипоевая кислота проявляет хеллаторные свойства к Сd2+) и выводить их из организма [21—23]. Отмечена также способность a-липоевой кислоты восстанавливать глутатион и активировать выведение с желчью метилртути и цинка [24]. Вместе с тем, дигидролипоевая кислота может проявлять прооксидантные свойства, восстанавливая Fe3– в Fe?+, образуя реактивные серусодержащие радикалы, способные повреждать такие протеины, как креатинкиназа, a-1-антипротеиназа.
Имеются непрямые доказательства вовлечения взаимодействия ЛК/ДГЛК с железом в цитопротекторные эффекты липоевой кислоты. Так, известно, что присутствие железа, образование его комплексов с ДНК является непременным условием свободно-радикального повреждения ДНК, а предварительная обработка хелаторами (ЭДТА) предотвращает восприимчивость ДНК к повреждению. Наблюдали также устранение протекторного действия липоевой кислоты по отношению к повреждению ДНК в результате предварительной инкубации с ЭДТА, что указывает на вклад взаимодействия липоевой кислоты с железом в её протекторные эффекты.
Аналогами a-липоевой кислоты являются тиоктовая кислота, липамид, витамин N (биотин), эспа-липон, берлитион, тиогама (мегламиновая соль a-липоевой кислоты) и др. [18]. a-Липоевую кислоту из-за её сходства с жирной кислотой часто называют тиоктовой кислотой ("тио-" — означает соединение серы, "-октовая кислота" — кислота с 8 атомами углерода).
Липамид (амид липоевой кислоты) — кристаллический порошок светло-жёлтого цвета; практически нерастворим в воде, мало растворим в спирте [10, 11, 15].
Структурная формула:
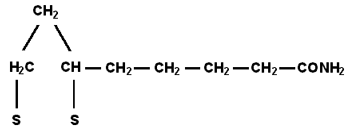
Биотин (витамин N) — кристаллическое вещество, хорошо растворимое в воде и спирте; устойчивое соединение, биологическая активность которого очень велика и не меняется при кипячении растворов и доступе кислорода. Суточная активность человека в биотине, по-видимому, не превышает 150—200 мкг/сут.
Нарушение обмена и недостаточность биотина наблюдаются при себорейном дерматите у грудных детей (болезнь Лейнера), сахарном диабете, остром и хроническом гепатитах. Назначение биотина по 400 мкг в день предотвращало развитие холестеринового атеросклероза у кроликов. Лечебные дозы биотина снижали содержание общего холестерина и a-липопротеидов в крови у больных атеросклерозом, а также уменьшали выведение тиамина и аскорбиновой кислоты. Биотин в опытах на животных не оказал токсического действия даже в значительных дозах [2].
Структурная формула:
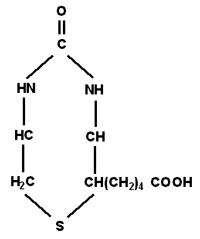
Эспа-липон — высокоочищенный энантомер, близкий по своей активности к природному (фирма "Эспарма" Германия). Берлитион — этилендиаминовая соль a-липоевой кислоты (фирма "Берлин-Хеми АГ/ группа Менарини/".
Клинические апробации препаратов a-липоевой кислоты в первую очередь доказали их высокую эффективность при лечении диабетических поражений нервной системы [4]. Многочисленные исследования подтвердили высокую эффективность этих препаратов при лечении диабетической дистальной полинейропатии, энцефалопатии, синдрома диабетической стопы, диабетической автономной нейропатии сердца и желудочно-кишечного тракта, эректильной дисфункции и диабетической ретинопатии. Применение липоевой кислоты способствует восстановлению болевой, температурной, вибрационной и тактильной чувствительности, уменьшению боли, парестезий, площади и глубины трофических язв, улучшает общее состояние больного. Получены положительные результаты использования a-липоевой кислоты при патологии щитовидной железы (гипотиреоз, аутоиммунный тиреоидит) в качестве иммуномодулятора и средства, позволяющего повысить чувствительность периферических тканей к тиреоидным гормонам [6, 7, 9, 16].
Вместе с тем, остались недостаточно экспериментально и клинически исследованными такие стороны действия a-липоевой кислоты и её аналогов, как детоксицирующий эффект при интоксикациях солями тяжёлых металлов.
В последние десятилетия среди химических загрязнителей окружающей среды глобального, регионального и локального значения свинец (Pb) занимает одно из центральных мест. Вследствие его широкого распространения в объектах окружающей среды, высоких кумулятивных свойств и политропного характера токсического действия, его влияние на организм людей приводит к развитию профессиональных и экологически обусловленных заболеваний экзохимической природы. Несмотря на то, что в последние десятилетия активно изучались и продолжают исследоваться различные аспекты действия металла на живой организм, проблема терапии свинцовой интоксикации остаётся одной из актуальных [14, 15].
Обусловленная действием тяжёлых металлов или их комбинацией с пестицидами и ионизирующим излучением, неблагоприятная экологическая обстановка требует разработки лечебных и особенно профилактических мероприятий, направленных на улучшение и сохранение здоровья людей.
В этом аспекте использование традиционной медикаментозной терапии далеко не всегда обосновано. Это обусловлено как интенсивною химизацией производства и быта, так и повышенным использованием лекарственных средств и изменением в питании людей (широкое использование консервантов, красителей и т.д.), которые вызвали увеличение частоты распространения аллергических заболеваний. Синтезированные ранее вещества с протекторными возможностями имеют определённую токсичность и становятся неэффективными при длительном воздействии негативных факторов, в первую очередь малой интенсивности.
Известно большое количество комплексообразующих соединений, которые выводят тяжёлые металлы из организма. Наиболее распространённые из них — ЭДТА, сукцимер, унитиол, N-ацетилцистеин, амид липоевой кислоты и т.д.
2,3-Димеркаптоянтарная кислота (сукцимер) стала одним из эффективнейших детоксицирующих агентов при хронических интоксикациях тяжёлыми металлами [1].
Учитывая антиоксидантные свойства a-липоевой кислоты, её способность связывать металлы, эффективность при лечении сахарного диабета, токсического и вирусного гепатита, нами была проведена работа по изучению препарата Берлитион® 300 ораль фирмы "Берлин-Хеми АГ/Менарини группа/", который представляет собой этилендиаминовую соль a-липоевой кислоты, как средства детоксикации при хронической свинцовой интоксикации.
В группу больных с хронической свинцовой интоксикацией (у 14 — выраженная форма, у 6 — начальная) входили 13 мужчин и 7 женщин. Средний возраст больных составил 49,0±1,51 лет; стаж работы в условиях воздействия свинца — 18,5±1,36 года; средний постэкспозиционный период — 4,76±1,04 года.
Наряду с клиническим обследованием до и после окончания лечения оценивалось состояние периферической крови, показатели функциональной активности печени, белковый, липидный, углеводный, порфириновый обмен с использованием унифицированных методов.
Содержание свинца в цельной крови, железа в сыворотке крови, свинца и железа в моче определяли до и после окончания лечения. В моче уровень этих металлов определяли также на
С помощью реактивов фирмы "SIGMA" у 8 больных сатурнизмом было изучено содержание железа в сыворотке крови, общая железосвязывающая способность сыворотки крови (ОЖСС) и степень насыщения трансферрина железом (% НТЖ).
У 15 больных с полинейропатией исследовали скорость проведения импульса (СПИ) по сенсорным волокнам срединного и локтевого нервов правой руки до и после курса лечения препаратом Берлитион 300 ораль с помощью метода стимуляционной электромиографии (ЭНМГ).
Препарат Берлитион 300 ораль больные принимали в виде таблеток в течение 10 дней, в первые 3 дня по 300 мг 2 раза в день, последующие 7 дней по 300 мг 1 раз в день после еды.
Выведение свинца с мочой у больных сатурнизмом повышалось к 8 дню за счет увеличения суточного диуреза. К
Изменения суточного выведения железа с мочой и снижение средних показателей содержания железа в сыворотке крови и свинца в крови недостоверны.
Остальные показатели, в том числе белковые фракции, состав периферической крови в процессе лечения больных сатурнизмом не изменялись.
Характер изменений в содержании свинца в крови и железа в сыворотке крови зависит от их исходного (до лечения) уровня, и чем он выше, тем заметнее уменьшение в результате лечения. Верхний исходный уровень свинца в крови, при котором отмечено его достоверное снижение в процессе лечения, составляет 40 мг/л, т.е. верхний предел допустимого содержания свинца в крови для работающих мужчин. Существенное понижение содержание железа в сыворотке крови отмечено в группе лиц, у которых его уровень был выше 30 мг/л.
Результаты ЭНМГ показали, что у больных исследуемой группы наблюдалось значительное снижение исходной СПИ в дистальных отделах срединного и локтевого нервов. Особенно выраженным это снижение было в дистальном отрезке срединного нерва (среднее значение СПИ в группе испытуемых было меньше нижней границы
После 10-дневного курса лечения препаратом Берлитион 300 ораль в дозе 600—300 мг/сут наблюдалось статистически достоверное увеличение СПИ по сенсорным волокнам в дистальном отделе срединного нерва и тенденция к увеличению СПИ в дистальном отделе локтевого (р=0,06), что свидетельствует о развитии в исследуемых нервах процессов ремиелинизации и улучшении аксонального проведения нервных импульсов.
Все больные были выписаны из стационара с улучшением состояния, уменьшением неприятных ощущений и болей в руках и ногах, увеличением мышечной силы, побочные эффекты не зарегистрированы.
Таким образом, результаты клинических исследований показали, что 10-дневный курс лечения больных хронической свинцовой интоксикацией Берлитионом 300 ораль оказывает благоприятное влияние на течение заболевания, не вызывая каких-либо негативных побочных эффектов. Препарат может быть рекомендован как средство антидотной терапии при хронической свинцовой интоксикации [12].
Литература
1. Архипова О.Г., Зорина Л.А., Соркина Н.С. Комплексоны в клинике профессиональных заболеваний. —М.: Медицина, 1975. —С. 62.
2. Збарский Б.И., Иванов И.И., Мардашов С.Р. Биологическая химия. —Ленинград.: "Медицина", 1972. —С. 182—185.
3. Зуєва Н.О., Маньковский Б.М., Овсянікова Л.М. та ін. Вплив лікування берлітіоном (a-ліпоєвая кислота) на концентрацію інсуліну та показники антиоксидантного статусу в крові ліквідаторів наслідків аварії на ЧАЕС // Врачебная практика. —1999. —№1. —С. 86—88.
4. Звягина Л.А. Применение a-липоевой кислоты (препарат Эспа-липон) для лечения больных с хроническим нарушением мозгового кровообращения // Фармакол. вісник. —2000. —№6. —С. 22—24.
5. Кундиев Ю.И., Лубянова И.П., Михайлик О.М. и др. Лампека. — Препарат a-липоевой кислоты Берлитион 300 ораль как средство коррекции изменений в организме, связанных с гиперферремией // Там же. —С. 6—9.
6. Кірієнко Д.В., Пешко А.О., Щербак О.В. Терапевтична ефективність a-ліпоєвої кислоти (Еспа-ліпону) при аутоімунному тиреоідиті з гіпотиреозом // Ліки. —2002. —№3—4. —С. 112—115.
7. Кіндій Т.В. Використання ЕСПА-ЛІПОНУ в комплексному лікуванні початкової ретинопатії // Ліки. —2000. —№5. —С. 17—18.
8. Козачок Н.Н., Селюк М.Н. Применение липоевой кислоты (берлитиона) в клинической практике // Мистецтво лікування. —2003. —№5. —С. 75—77.
9. Кірієнко Д.В., Боднар П.М., Щербак О.В. Терапія препаратами ?-ліпоєвої кислоти (Еспа-ліпоном) діабетичної автономної невропатії серця // Ліки. —1998. —№2. —С. 19—24.
10. Лескова Г.Е. Защитный эффект амида липоевой кислоты при экспериментальном меркуриализме // Гигиена труда и проф. заболевания. —1979. —№6. —С. 27—30.
11. Логинов А.С. и др. Эффективность амида липоевой кислоты при хронических заболеваниях печени // Сов. Мед. —1970. —№1. —С. 47—50.
12. Лубянова И.П., Харченко Т.Д., Вознесенский С.А. и др. Берлитион как средство детоксикации при хронической свинцовой интоксикации // Ліки. —України. —2000. —№10. —С. 35—37.
13. Трахтенберг І.М., Луговський С.П. Нові експериментальні дані щодо мембранної концепції патогенезу свинцевої інтоксикації: клітинні і субклітинні аспекти. Тези доповідей II з?їзду токсикологів України. —Київ, 2004. —С. 31—32.
14. Трахтенберг І.М. Пріоритетні аспекти фундаментальних досліджень у токсикології. —Там же. —С. 8—9.
15. Трахтенберг И.М., Лескова Г.Е., Верич Г.Е. О защитном действии амида липоевой кислоты при интоксикации ртутноорганическими соединениями // Гигиена труда и проф. заболевания. —1974. —№9. —С. 25—27.
16. Ткач С.М., Кліменко О.П. Прискорення скоротливої активності жовчного міхура під впливом ?-ліпоєвої кислоти у хворих з діабетичним холецистопарезом // Ендокринологія. —2001. —Т. 6, №2. —С. 152—159.
17. Хворостинка В.Н., Бобронникова Л.Р. Клиническая эффективность a-липоевой кислоти (берлитиона 300) при хронических токсических заболеваниях печени // Мистецтво лікування. —2004. —№2. —С. 60—62.
18. Щербак О.В. Сучасний фармацевтичний ринок препаратів альфа-ліпоєвої кислоти в Україні // Фармацевтичний журнал. —2000. —№4. —С. 29—32.
19. Packer L., Witt E.H., Trischler H.J. Alfa-Lipoic acid as a biological antioxidant // Free Radic Biol Med. —1995. —V. 19, N2. —P. 227—50.
20. Hagen T.M., Ingersoll R.T., Lykkesfeldt J. et al. (R)-alfa-lipoic acid-supplemented old rats have improved mitochondrial function, decreased oxidative damage, and increased metabolic rate // FASEB J. —1999. —V. 13, N2. —P. 411—8.
21. Biewenga G.P., Haenen G.R., Bast A. The pharmacology jf the antioxidant lipoic acid // Gen Pharmacol. —1997. —V. 29, N3. —P. 315—31.
22. Gregus Z., Stein A.F., Varga F., Klaassen C.D. Effect of lipoic acid on biliary excretion of glutathione and metals // Toxicol Appl Pharmacol. —1992. —V. 114, N1. —P. 88—96.
23. Ou P., Tritschler H.J., Wolff S.P. Thioctic (lipoic) acid: a therapeutic metalchelating antioxidant? // Biochem Pharmacol. —1995. —V. 29, N 50. —P. 123—126.
24. Scott B.C., Aruoma O.I., Evans P.J. et al. Lipoic and digydrolipoic acids as antioxidants. A clinical evaluation // Free Radic Res. —1994. —V. 20, N2. —P. 119—33.