ТОКСИКОЛОГІЯ ПЕСТИЦИДІВ
УДК 615.9:616.15
ДОСТИЖЕНИЯ В ОБЛАСТИ ИЗУЧЕНИЯ ВЛИЯНИЯ ПЕСТИЦИДОВ НА СИСТЕМУ КРОВЕТВОРЕНИЯ
В.Г. Шуляк., к.б.н.
Институт экогигиены и токсикологии им. Л.И.Медведя, г. Киев
Изучение морфологического состава периферической крови всегда проводилось в комплексе токсикологических исследований пестицидов при их гигиеническом нормировании.
Ранее считали [1-10], что изменения периферической крови при воздействии пестицидов являются интегральным показателем, отражающим общетоксическое действие на организм, т.е. пестициды не оказывают непосредственного влияния на систему кроветворения. Однако в литературе встречались данные о развитии гематологических заболеваний (полидефицитные, пернициозная, гипо- и апластическая анемии, агранулоцитоз, миелобластическая лейкемия) [11-18] у людей в результате контакта с некоторыми пестицидами.
По мере накопления экспериментальных данных стало очевидным, что не все изменения в периферической крови при воздействии некоторых пестицидов можно объяснить их общетоксическим действием.
Нами были проведены комплексные углубленные исследования, которые включали изучение показателей периферической крови, кроветворения в костном мозге, селезенке и морфофункционального статуса лейкоцитов крови при воздействии фосфорорганических пестицидов (ФОП) [19]. Было изучено влияние на систему крови 7 ФОП различного химического строения (ДДВФ, актеллик, хостаквик, гетерофос, мирал, циклофос, плондрел) в острых и хронических экспериментах при различных путях поступления в организм (пероральном и ингаляционном).
Результаты исследований показали, что некоторые из ФОП оказывают непосредственное влияние на процессы кроветворения в костном мозге, вызывая стимуляцию или угнетение одного, нескольких или всех ростков кроветворения. Среди них выявлены ФОП, оказывающие выраженное угнетающее действие на систему крови. Так, плондрел при пероральном воздействии как в остром (1/2 ЛД50 и 1/5 ЛД50, трехкратно), так и в хроническом (1/100, 1/1000 ЛД50 в течение 6 мес) экспериментах вызывал депрессию костномозгового кроветворения на уровне полипотентной клетки-предшественницы всех ростков гемопоэза. В результате развивалась аплазия эритро-, гранулоцито- и тромбоцитопоэза и жировое замещение очагов гемопоэза. Пероральное и, особенно, ингаляционное поступление в организм циклофоса в больших и малых дозах приводило к гемолитическому эффекту с циркуляцией макрофагов в сосудистом русле и неэффективному эритропоэзу в костном мозге. При действии обоих препаратов в селезенке развивалось заместительное экстрамедуллярное кроветворение [20].
Влияние на систему крови не было связано с наличием или выраженностью антихолинэстеразного эффекта у ФОП. В результате собственных исследований, а также анализа и сопоставления данных литературы было показано, что действие ФОП на систему гемопоэза обусловлено наличием в химической структуре пестицидов тех или иных функциональных групп [21].
Кроме того, проведено изучение изменений периферической крови у людей с острыми отравлениями ФОП (случайными и с суицидальной целью). Оказалось, что изменения в периферической крови людей и лабораторных животных на уровне влияния высоких доз ФОП имеют ту же направленность, однако у людей они более выражены. Нами изучено влияние на систему крови более 150 пестицидов и других химических веществ. Анализ результатов исследований позволил сделать ряд обобщений и высказать гипотезы, которые затем были подтверж
Для раскрытия механизма действия вещества и наиболее адекватной оценки получаемых результатов разработана схема постановки эксперимента по изучению гемотоксического действия пестицидов и других химических веществ [22]. Схема включает обязательное изучение влияния вещества при однократном поступлении в организм в токсических дозах (на уровне 1/2 ЛД50, однократно и 1/5 ЛД50, трехкратно). При этом необходимо изучить показатели периферической крови, цитохимический статус лейкоцитов крови, кроветворение в костном мозге и селезенке. При оценке показателей периферической крови в комплексe исследований, кроме общего развернутого анализа крови, необходимо определять количество ретикулоцитов и тромбоцитов, дабы охватить возможные изменения всех ростков гемопоэза. Исследования количественного и морфофункционального состава периферической крови необходимо проводить в динамике: через 1, 3, 7, 14 и 21 сут, костномозгового и селезеночного кроветворения — через 7, 14 и 21 сут после введения вещества. Указанные объем, дозы и сроки исследований позволяют понять возможный механизм действия вещества на систему крови и при этом охватить весь процесс кроветворения — от стволовой клетки костного мозга до пула зрелых циркулирующих клеток периферической крови.
Был подобран и внедрен комплекс цитохимических методов изучения состояния циркулирующих клеток крови всех генераций. Это позволило выявлять морфофункциональные изменения в клетках и, что особенно важно, оценивать степень их зрелости. В результате были разработаны методические подходы к прогнозированию изменений в костном мозге при воздействии пестицидов на основе морфофункционального статуса клеток периферической крови.
Кроме того, разработаны подходы к экстраполяции экспериментальных данных по гемотоксическому действию пестицидов на человека. Как оказалось, при действии некоторых пестицидов результаты изучения показателей периферической крови не всегда отражают депрессивное состояние костномозгового кроветворения. На уровне влияния малых доз пестицидов в хронических экспериментах изменения в периферической крови могут быть нерезкими или находиться в пределах физиологических колебаний. Нами высказана гипотеза, а затем для некоторых пестицидов подтверждено экспериментально, что указанное положение обусловлено развитием в организме грызунов защитного экстрамедуллярного кроветворения, которое компенсирует показатели периферической крови.
Некоторая активация селезеночного кроветворения является естественным процессом для половозрелых экспериментальных животных — крыс, мышей, морских свинок [23, 24]. Однако, у человека в норме экстрамедуллярное кроветворение имеет место только в эмбриональном периоде. У взрослых людей возниковение внекостномозговых очагов кроветворения наблюдается при диспластических и лейкозных процессах [25, 26]. Учитывая последнее, для адекватной эктраполяции на человека данных изучения гематоксического действия химических веществ, которые получены на грызунах, необходимо учитывать неполную адекватность этих экспериментальных моделей.
В течение последних 10 лет одним из направлений наших исследований было изучение влияния на систему крови и выяснение механизма гематоксического эффекта пестицидов при их изолированном и комбинированном поступлении в организм. Это направление является одним из приоритетных в токсикологии пестицидов.
Материалы и методы исследования
Изучали воздействие отдельных пестицидов — дециса, дурсбана, фоксима, хлорокиси меди, поликарбацина, а также смеси дециса с дурсбаном в соотношении 1:1, дециса с фоксимом в соотношении 1:1 и хлорокиси меди с поликарбацином в соотношении 1:3. Пестициды однократно вводили в желудок белых крыс Wistar массой тела 180-220 г в дозах 1/2 ЛД50.
Исследования проводили с помощью унифицированных гематологических методов [27]. Состояние системы крови оценивали по показателям периферической крови и кроветворения в костном мозге. При изучении морфологического состава периферической крови определяли концентрацию гемоглобина цианметгемоглобиновым методом с помощью гемоглобинометра ГФ-1, подсчитывали количество эритроцитов и лейкоцитов в камере Горяева, ретикулоцитов в мазках крови после суправитального окрашивания бриллианткрезиловым синим, тромбоцитов по методу Фонио, гемограммы с анализом морфологических изменений и нарушений структуры лейкоцитов и эритроцитов. Рассчитывали среднее содержание гемоглобина в эритроците.
О состоянии гемопоэза в костном мозге судили на основании подсчета общего количества миелокариоцитов в бедренной кости и миелограммы с анализом изменений структуры миелокариоцитов. Для оценки изменений в миелограмме были рассчитаны лейко-эритробластическое отношение, индексы зрелости эритрокариоцитов, нейтрофилов и эозинофилов.
Для изучения механизма действия на систему крови препаратов дурсбана, дециса и их комбинации проводили определение билирубина, осмотической резистентности эритроцитов, наличия нестабильного и фетального гемоглобина.
Изучение показателей периферической крови проводили на 1, 3, 7, 14 сут после введения препаратов и сравнивали с исходными данными, костного мозга — на 7 и 14 дни и сравнивали с контролем. Кроме того, для препаратов поликарбацин, хлорокись меди и их смеси исследования проводили на 21 сут после введения.
Результаты и их обсуждение
Хлорокись меди и поликарбацин при их изолированном поступлении в организм приводят к значительной анемии. Механизм развития анемизирующего эффекта у них разный.
При действии хлорокиси меди начиная с 3 сут снижались на 20 % количество эритроцитов и на 15 % уровень гемоглобина, отмечались резкий ретикулоцитоз, анизоцитоз и слабая полихромазия эритроцитов, наличие в периферической крови единичных оксифильных нормоцитов. Выявлены лейкопения без достоверных изменений в лейкограмме и тромбоцитопения. Количество эритроцитов и тромбоцитов не восстанавливалось даже на 21 сутки. Нарушений в костном мозге при этом не выявлено.
Поликарбацин приводит к более выраженной анемии: количество эритроцитов уменьшается на 29% без изменений уровня гемоглобина, отмечается резкий ретикулоцитоз, выраженный анизоцитоз эритроцитов. Анемические проявления сохраняются до конца срока исследований. На 21 сут развивается ретикулоцитопения. Количество тромбоцитов уменьшается в 6 раз и не восстанавливается в течение всего эксперимента. В белой крови наблюдается дегенеративный нейтрофилез, хроматинолиз и полисегментоз ядер нейтрофилов, моноцитоз, эозинопения и лимфоцитопения, а позже — лейкопения.
В миелограмме отмечаются признаки нерезкого угнетения эритропоэза: уменьшается общее количество элементов эритроидного ростка за счет полихроматофильных нормоцитов. Это сопровождается слабой вакуолизацией очагов гемопоэза в костном мозге и увеличением количества лимфоидных элементов.
Таким образом, поликарбацин при изолированном поступлении в организм приводит к слабому торможению эритро- и гранулоцитопоэза в костном мозге.
При введении в желудок смеси хлорокиси меди и поликарбацина отмечались существенно меньшие изменения показателей красной крови, которые восстанавливались на 14 сут наблюдения. Однако тромбоцитопения и моноцитоз с наличием промоноцитов в лейкограмме выявлялись в течение всего исследования.
При изучении кроветворения в костном мозге нарушений эритропоэза не наблюдалось. Увеличивалось количество промоноцитов, эозинофильных метамиелоцитов, что свидетельствует об активации соответствующих ростков гемопоэза. Количество мегакариоцитов в миелограмме остается без изменений, что указывает на перераспределительный характер выявленной в периферической крови тромбоцитопении.
Таким образом, при действии смеси хлорокиси меди и поликарбацина анемизирующий эффект отдельных препаратов не проявляется и компенсируется, вероятно, за счет стимуляции эритропоэза хлорокисью меди [28].
При острой интоксикации децисом вначале наблюдался ретикулоцитоз без изменений уровня гемоглобина и количества эритроцитов. На 14 день количество эритроцитов несколько уменьшилось, а ретикулоцитов восстановилось. Число тромбоцитов достоверно не изменялось. В лейкограмме выявлены нейтрофильный лейкоцитоз со сдвигом влево и относительная лимфоцитопения. Количество моноцитов было подвержено колебаниям. В периферическую кровь выходили единичные макрофаги, оксифильные и полихроматофильные нормоциты (7 сут), эритроциты с патологическими остатками ядра (14 сут). Выявлены изменения морфологии лейкоцитов в виде гиперсегментоза нейтрофилов и пикноза лимфоцитов. Наблюдалось некоторое снижение осмотической резистентности эритроцитов. Уровень нестабильного и фетального гемоглобина не изменялся.
Общее количество миелокариоцитов в костном мозге не изменялось. Количество эритрокариоцитов в первые 7 дней имело тенденцию к увеличению, но на 14 сут было установлено слабое угнетение эритропоэза. Гранулоцитопоэз несколько угнетался: количество палочкоядерных нейтрофилов снижено, отмечены также признаки разрушения их поздних генераций в виде кариолиза и хроматинолиза. Количество эозинофильных элементов, моноцитов и плазмоцитов было также уменьшено.
Следовательно, острая интоксикация децисом вызывает слабый анемизирующий эффект с нерезким угнетением эритропоэза и патологической регенерации крови.
Внутрижелудочное поступление дурсбана приводило на 3 день к снижению содержания гемоглобина (на 8-11 %) без изменения количества эритроцитов. Уровень гемоглобина не восстанавливался даже на 14 сут. Анемизирующий эффект сопровождался выраженным ретикулоцитозом (увеличение на 65-68 %). Имели место нарушения морфологии эритроцитов в виде выраженного микросфероцитоза и анизоцитоза. На 14 сут в периферической крови выявлены единичные мегалоциты. Общее количество лейкоцитов слабо уменьшено только на 14 сут. В лейкограмме изменений количественного соотношения лейкоцитов не наблюдалось, однако выявлены морфологические изменения: хроматинолиз нейтрофилов, повышенное количество клеток лейколиза и атипичные формы лимфоцитов. Число тромбоцитов достоверно не изменялось.
Осмотическая резистентность эритроцитов несколько снижалась. Содержание нестабильного гемоглобина не изменялось, а фетальный гемоглобин повышался на 70 %.
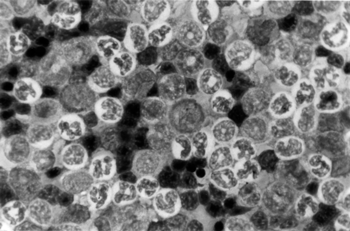
Рисунок 1. Костный мозг интактных крыс. х 1000
В костном мозге общее количество миелокариоцитов было без изменений. Однако в миелограмме, наряду с уменьшением количества созревающих клеток эритрона, отмечалось выраженное (в 22 раза) повышение количества недифференцируемых бластов и умеренное увеличение диаметра эритробластов (рис. 1, 2). Кроме того, увеличивалось число молодых клеток нейтрофильного и эозинофильного ростков — миелобластов и промиелоцитов.
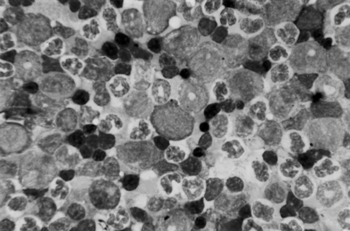
Рисунок 2. Костный мозг белых крыс при воздействии дурсбана (14 сут). Макроформы эритобластов. х 1000.
Таким образом, изолированное поступление в организм дурсбана приводит к слабой анемии и регенерации эритропоэза по макроцитарному типу.
При комбинированном действии дециса и дурсбана наблюдались снижение (на 14 и 13 % на 3 и 7 сут, соответственно) уровня гемоглобина и ретикулоцитоз (повышение на 56 % только на 1 сут). Количество эритроцитов не изменялось. Однако были выявлены выраженный макроцитоз, анизоцитоз и полихромазия эритроцитов. В периферическую кровь выходили базофильные и оксифильные нормоциты. В белой крови обнаружены моноцитопения, относительный нейтрофилез со сдвигом влево и повышение количества атипичных лимфоцитов.
Осмотическая резистентность эритроцитов и уровень нестабильного гемоглобина не изменялись. Резко возрастало (на 194 %) содержание фетального гемоглобина в эритроцитах.
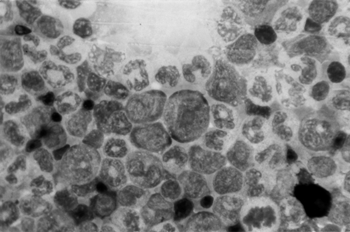
Рисунок 3. Костный мозг белых крыс при воздействии смеси дециса и дурсбана (14 сут). Макроформы эритобластов. х 1000.
В костном мозге на 14 сут выявлена активация всех ростков кроветворения на уровне молодых клеточных генераций. Установлено значительное увеличение диаметра эритробластов (рис. 3). По всем полям зрения выявлялись гигантские формы эритробластов (рис. 4).
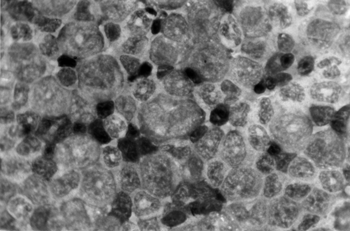
Рисунок 4. Костный мозг белых крыс при воздействии смеси дециса и дурсбана (14 сут). Гигантский эритробласт. х 1000.
Регенерация крови при действии смеси дециса и дурсбана осуществляется по пути возврата к эмбриональному типу кроветворения [29].
Однократное пероральное введение фоксима приводило на 7 сут к эритроцитопении (на 19 %) без изменения уровня гемоглобина, повышению среднего содержания гемоглобина в эритроците на 28 %. На 14 сут число эритроцитов и уровень гемоглобина возрастали. В лейкограмме отмечались фазовые колебания числа моноцитов, снижение количества палочкоядерных форм нейтрофилов, наличие лимфоцитов с атипичным строением ядра, а затем (на 14 сут) компенсаторный выброс пролимфоцитов.
В костном мозге на 7 сут наблюдалась стимуляция эритроидного ростка в ответ на эритроцитопению в периферической крови. На это указывали увеличение общего числа клеток эритрона (за счет повышенного содержания полихроматофильных нормоцитов и клеток деления) и снижение лейко-эритробластического отношения. На 7 и 14 сут наблюдалось уменьшение продукции клеточных элементов моноцитарного, эозинофильного и нейтрофильного ростков кроветворения, хроматинолиз и вакуолизация ядер и цитоплазмы нейтрофильных промиело-, миело- и метамиелоцитов. Количество пролимфоцитов в костном мозге уменьшалось за счет усиленного вымывания их в периферию.
Таким образом, фоксим вызывает нерезкую стимуляцию и напряжение эритрона и слабое угнетение гранулоцито- и моноцитопоэза.
При поступлении в организм смеси дециса и фоксима в периферической крови выявлялись резкая ретикулоцитопения (3 сут, повышение в 4 раза) без изменения количества эритроцитов и уровня гемоглобина, а также эритроциты с патологическими остатками ядер, единичные пронормоциты и базофильные нормоциты. В белой крови — лейкоцитоз без изменений соотношения лейкоцитов в лейкограмме, наличие пролимфоцитов и атипичных форм лимфоцитов. На 3-14 сут исследований регистрировали тромбоцитопению.
В мазках костного мозга по всем полям зрения выявлялось опустошение очагов кроветворения и замещение их жировой тканью. Общее количество миелокариоцитов снижалось на 31 % (14 сут). В миелограмме определялись признаки угнетения эритропоэза: количество эритробластов, базофильных нормоцитов снижалось, повышался индекс созревания эритрокариоцитов. Лейко-эритробластическое отношение в миелограмме увеличено. Отмечалось также некоторое торможение пролиферации клеток нейтрофильного и моноцитарного ростков. Повышалось число тучных клеток.
Как следудет из полученных данных, при острой интоксикации смесью дециса и фоксима вначале (на 7 сут) отмечается некоторая стимуляция и напряжение эритроидного ростка. Наблюдаемые в периферической крови изменения обусловлены патологической регенерацией элементов эритроидного и нейтрофильного ростков. На 14 сут развивается гипопластический процесс с депрессией эритро- и гранулоцитопоэза [30, 31].
Таким образом, некоторые из изученных комбинаций пестицидов (поликарбацин и хлорокись меди) не оказывают потенцирующего действия на процессы кроветворения, а влияют по типу антагонизма.
Совместное поступление в организм дециса с дурсбаном и фоксимом вызывает значительно более выраженные изменения в системе крови по сравнению с изолированным их действием. Потенцирующий эффект при комбинированном действии дециса и дурсбана приводит к развитию кроветворения, которое осуществляется по эмбриональному пути, дециса и фоксима — к выраженному гипопластическому процессу.
Гипопластические состояния костномозгового кроветворения являются одним из тяжелых заболеваний системы крови, лечение которых до сих пор остается нерешенной проблемой [32, 33]. Кроме того, гипопластические анемии иногда являются прелейкемической формой гемобластозов и предшествуют бластной трансформации костномозгового кроветворения [26, 34].
В связи с полученными результатами, изучение комбинированного действия пестицидов на систему крови является важной задачей дальнейших исследований, которые позволят предупредить развитие заболеваний системы крови у людей, контактировавших с некоторыми комбинациями пестицидов.
Литература
1. Стацек Н.К. Материалы по токсикологии метилсистокса и его гигиеническому нормированию. Автореф. дисс. ... канд. мед. наук. —Киев, 1960. —18 с.
2. Каган Ю.С. Токсикология фосфорорганических инсектицидов и гигиена труда при их применении. —М., 1963. —325 с.
3. Паньшина Т.Н. Материалы по токсикологии фосфамида и гигиеническому нормированию его содержания в воздухе рабочей зоны. Автореф. дисс. ... канд. мед. наук. —Киев, 1964. —15 с.
4. Таращук В.В. Некоторые биохимические и морфологические изменения в нервной системе и периферической крови при остром отравлении метилсистоксом. Автореф. дисс. ... канд. мед. наук. —Киев, 1967. —21 с.
5. Сасинович Л.М. Материалы по токсикологии диметилдихлорвинил фосфата (ДДВФ) и по гигиенической характеристике условий его применения. Автореф. дисс. ... канд. мед. наук. —Киев, 1968. —20 с.
6. Матюшина В.И. Токсикология метилнитрофоса и вопросы гигиены труда при его применении в сельском хозяйстве. Автореф. дисс. ... канд. мед. наук. —Киев, 1968. —16 с.
7. Крайнюков И.Н. Изменения периферической крови при отравлении карбофосом // Сборник научных работ Куйбышевского мед. института —Куйбышев, 1969. —Вып. 2. —С. 177-178.
8. Медовар А.М. Экспериментальные данные о влиянии сайфоса на некоторые биохимичиеские и морфологические показатели крови // Гигиена применения, токсикология пестицидов и клиника отравлений. —Киев: ВНИИГИНТОКС, 1969. —Вып. 7. —С. 327-331.
9. Болотный А.В. Токсикология нового фосфорорганического инсектицида гардоны и обоснование гигиенических регламентов его применения. Автореф. дисс. ... канд. мед. наук. —Киев, 1973. —27 с.
10. Ахмеджанов К. Состояние некоторых показателей периферической крови при воздействии фосфорорганических соединений малой интенсивности в эксперименте // Актуальные вопросы гигиены применения пестицидов в различных климато-географических зонах. —Ереван: Айастан, 1976. —С. 129-131.
11. Польченко В.И. Отравления пестицидами по данным мировой литературы // Гигиена применения, токсикология пестицидов и клиника отравлений: Материалы 4-ой Всес. науч. конф. по гигиене и токсикологии пестицидов, 11-14 июня 1968 г. —Киев: ВНИИГИНТОКС, 1968. —Вып. 6. —С. 61-72.
12. Каган Ю.С. Общая характеристика отравлений /Под ред. М.Л.Тараховского/. —Киев: Здоров`я, 1973. —С. 5-14.
13. Буркацкая Е.Н., Лысина Г.Г., Карпенко В.Н. Лабораторная диагностика интоксикаций пестицидами. —М.: Медицина, 1978. —128 с.
14. Справочник по профессиональной патологии /Под ред. Л.Р.Грацианской, В.Е.Ковшило/. —Л.: Медицина, 1981. —373 с.
15. Rugman F.P., Cossick R. Aplastic anemia associated with organochlorine pesticide: case reports and review of evidence. —J. Clin. Pathol. —1990. —43(2). —P. 98-101.
16. Konopska L., Gorski T., Zdiechowska H. et al. Spostrzezenia kliniczne dotyczace niedokrwistosci aplastycznej wywolanej przez weglowodory chlororganiczne. —Pol. tyg. lek. —1982. —37 (34-35). —P. 1003-1006.
17. Roberts H.J. Aplastic anemia and red cell aplasia due to pentachlorphenol. —South. Med. J. —1983. —76 (1). —P. 45 —48.
18. Morgan Donald P., Stockdale Earl M., Roberts Robert J. et al. Anemia associated with exposure to lindane. —Arch. Environ Health —1980. —35 (5). —P. 307—310.
19. Шуляк В.Г. Влияние фосфорорганических пестицидов на гемопоэз. Автореф. дисс. ... канд. биол. наук. —Киев, 1989. —22 с.
20. Шуляк В.Г. Принципы экспериментальной оценки гематотоксического действия пестицидов на примеpе влияния циклофоса и плондрела на систему крови //Гигиена применения, токсикология пестицидов и полимерных материалов. —Киев, 1989. —Вып. 19. —С. 130-134.
21. Shulyak V.G. Hematologic effects of some pesticides, depending on chemical structure //Pharmacology and Toxicology. EUROTOX,97, Diversification in Toxicology: Man and Environment. —Aarhus, Denmark, June 25-28, 1997. —P. 111-112.
22. Шуляк В.Г. Методологічні підходи до оцінки гематотоксичної дії пестицидів при їх гігієнічному нормуванні //Актуальні проблеми екогігієни і токсикології: Матеріали науково-практичн. конф. 28-29 травня 1998. —Київ. —Ч. 1. —С. 246-249.
23. Maximow A., Bllom W. A textbook of histology. —London, 1957. —P. 194-198.
24. Дымшиц Р.А., Захаров Ю.M., Недоспасов В.О. и др. Селезенка и эритропоэз //Вопросы реактивности физиологических систем организма. Материалы 8 конф. Уральского межобластн. об-ва патофизиологов. —Свердловск, 1972. —С. 13-15.
25. Выговская Я.И., Логинский В.Е., Мазурок А.С. Гематологические синдромы в гематологической практике. —Киев: Здоров`я, 1981. —С. 296.
26. Гаврилов О.К., Файнштейн Ф.Э., Турбина Н.С. Депрессии кроветворения. —М.: Медицина, 1987. —256 с.
27. Лабораторные методы исследования в клинике. Справочник /Под ред. Меньшикова В.В. —М.: Медицина, 1987. —365 с.
28. Шуляк В.Г. Вплив хлороркису міді та полікарбацину на систему крові при ізольованій та комбінованій дії на організм //Environmental and Occupational Health and Safety in Agriculture on the Boundary of TWO Millennia Internatinal Conference under the Aegis of WHO, ILO and IAAMRH. Kyiv, Ukraine, September 8-11, 1998. —Institute of Occupational Health of the Academy of Medical Sciences of Ukraine —Kyiv, 1998. —Р. 79-80.
29. Shulyak V.G. The recurense to embryonic type of hemopoiesis resulting from chlorpyrifos and decis combined action //Toxicology Letters. Chemicals Safety for the 21st Century. Abstracts of the International Congress of Toxicology —ICT VIII. —Paris, 5-9 July 1998. —Suppl. 1/95 (1998). —Р. 146.
30. Shulyak V.G. Hypoplasia of bone marrow as result of combined influence of phosphororganic pesticides and pyrethroides //6th Intern. congress European association for veterynary pharmacology and toxicology. —Edinburg, Scotland, August 7-11, 1994. —P. 78-79.
31. Shulyak V.G. Combined and isolated effect of pesticides on blood system //Health, Safety and Ergonomic Aspects in Use of Chemicals in Agriculture and Forestry. Processings of the XII Joint CIGR, IAAMRH, IUFRO intern. symp., 8-11 June 1993. —Kiev. —P. 219-224.
32. Лейкопении /В.А.Алмазов, В.В.Афанасьев, А.Ю.Зарицкий и др. —Л.: Медицина, 1981. —240 с.
33. Романова А.Ф. Гипопластическая и апластическая анемия. —Киев: Здоров`я, 1982. —151 с.
34. Турбина Н.С. Гемодепрессии —предлейкоз //Актуальные проблемы клинической онкологии. —М., 1982. —C. 177-178.